2023年5月17日,中國科學院深圳先進技術研究院合成生物學研究所細胞與基因線路設計中心魏平課題組與丹麥皇家科學院院長Mogens H. Jensen課題組合作在Cell Systems上發表研究論文“Coupled oscillator cooperativity as a control mechanism in chronobiology”,通過合成生物學方法構建了一種三元耦合振蕩系統,并結合數學模型,首次深入地探討了生命系統中多重耦合振蕩系統中的調控機理。

文章上線截圖
文章鏈接:https://doi.org/10.1016/j.cels.2023.04.001
物理世界中,多個振蕩波的相互疊加可能產生干涉條紋等復雜現象。事實上,周期振蕩式的動力學行為不僅出現在物理現象中,在生命系統內也廣泛存在。從生物鐘、體節發育、神經沖動,到細胞周期、免疫調控、信號轉導,生物系統中各組分的周期性變化幫助我們維持穩定的節律、產生正確的發育結構、對外界信息做出精準而定量的響應;在這些過程中,往往會涉及到多種振蕩信號之間的相互作用。這種復雜系統中蘊含著怎樣的調控原理,是一個重要卻難解的問題。
同頻振蕩波的干涉(圖片來自網絡)

小鼠體節發育中Hes7的行波(引自Yoshioka-Kobayashi et al., 2020)
圖1 物理系統與生物系統中的振蕩
早在17世紀,物理學家惠更斯就發現兩個相互耦合的鐘擺在特定條件下可以發生神奇的同步現象,對這類問題的研究促生了非線性動力學中著名的耦合振子模型(coupled oscillators)。這一模型可以預測兩個彼此關聯(或單向關聯)的振子在何種條件下產生鎖頻、多穩態極限環以及混沌。然而,經典耦合振子模型刻畫的只是振子數n=2的簡單情況,無法探討真實生物系統中當n≥3時多種振蕩信號同時存在帶來的復雜性。多個振子會使系統變得更混亂還是更穩定?這其中是否存在全新的調控機理? 探索這一問題不僅需要在理論模型上進行拓展,更需要簡潔明了、沒有干擾的實驗體系。

兩節拍器通過底部木板相互作用形成反相同步(圖片來自網絡)

大腸桿菌中的合成振蕩系統被周期性阿拉伯糖刺激所同步(引自Mondragón-Palomino et al., 2011)
圖2 機械系統與生物系統中的耦合振子
為了探究這一問題,本文作者對前期在酵母細胞中人工構建的NF-κB振蕩系統(Zhang et al., 2017)進行了改造,進一步增加了系統的復雜度,實現系統能夠受到兩種外部信號的控制。該系統的核心設計是基于人體細胞中的與免疫響應相關的NF-κB/IκB信號分子構成的負反饋線路,通過信號分子嫁接的方式,在酵母細胞中形成NF-κB的周期性激活過程。利用微流控芯片系統,作者可以精確編程兩種外部輸入信號的振蕩周期與強度,從而實現了2個部周期信號與1個內部周期信號相互作用的三振蕩系統,為研究生命過程中多振蕩耦合問題提供了可定量調控的活細胞實驗系統。
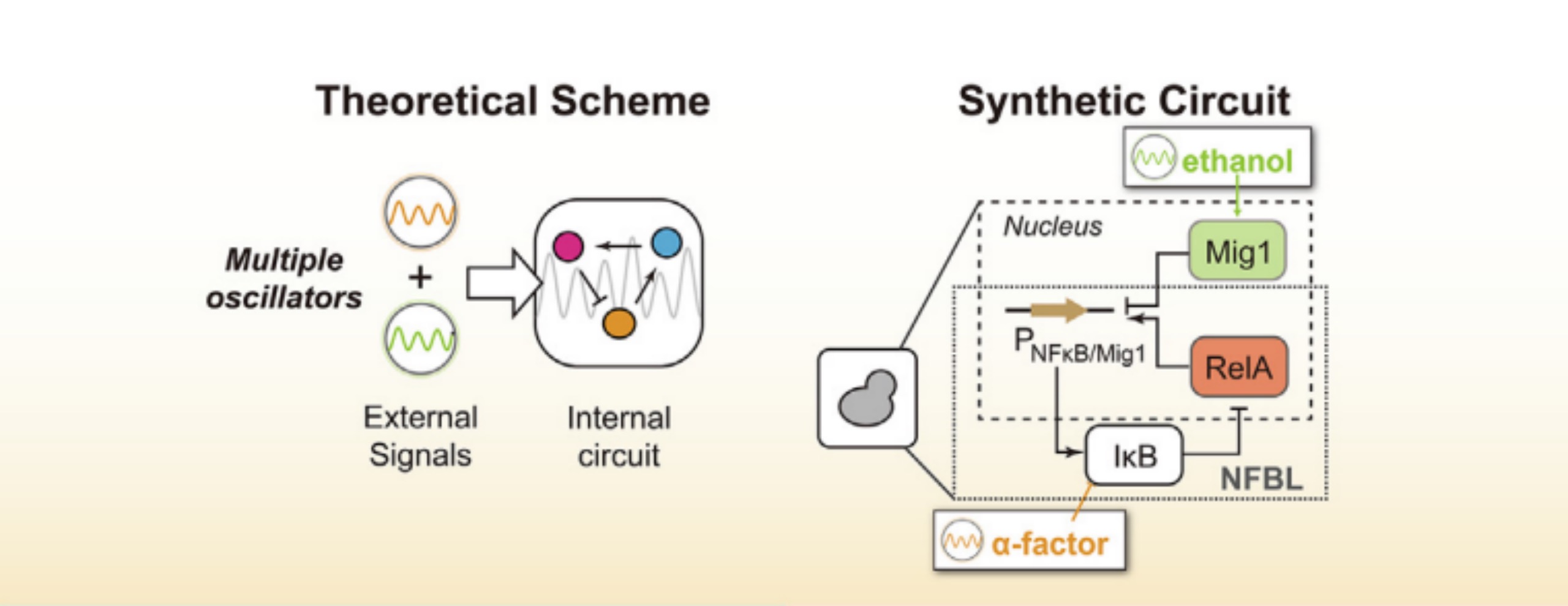
圖3 雙輸入振蕩系統的基本設計
基于這一系統結合數學模型,作者發現,雙重周期信號同時存在能夠顯著地提高內外振蕩同步化的范圍、降低細胞群體振蕩動力學的差異、提高同步化細胞在群體中所占的比例。模型模擬結果更表明,雙輸入條件能夠推遲混沌的發生。這些結果說明了外界兩種周期信號對系統的作用并不是簡單的線性疊加,而是以一種相互協同的形式產生作用。
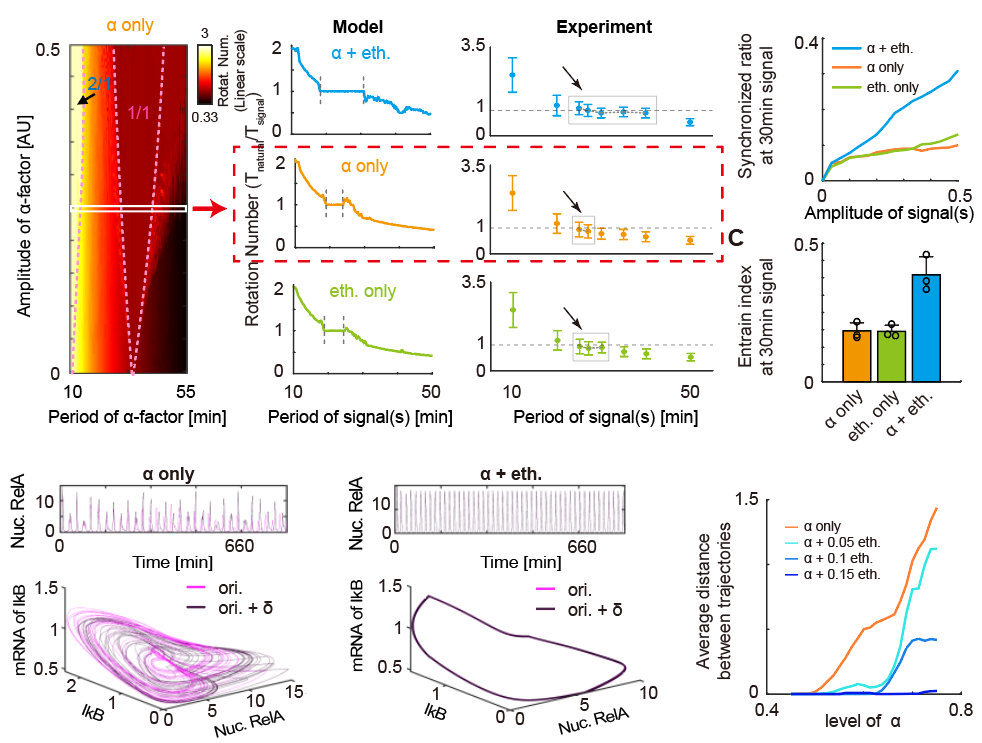
圖4 雙重周期信號擴大同步范圍、提高同步化細胞比例、延遲混沌發生
進一步,作者注意到調整外界信號間的相位差能夠非常明顯地改變內部振蕩的振幅,而保持內部振蕩周期不變,從而實現理論上嚴格的“調幅不調頻”。深入探究表明,帶來最大振幅的信號相位組合與內部系統的動力學參數之間存在高度相關性。為了驗證以上結論的普適性,作者還選取了三個不同的振蕩系統進行數值模擬。在范德波爾振子、p53振蕩系統和天然NF-κB振蕩系統中,以上結論均得到很好的重復。
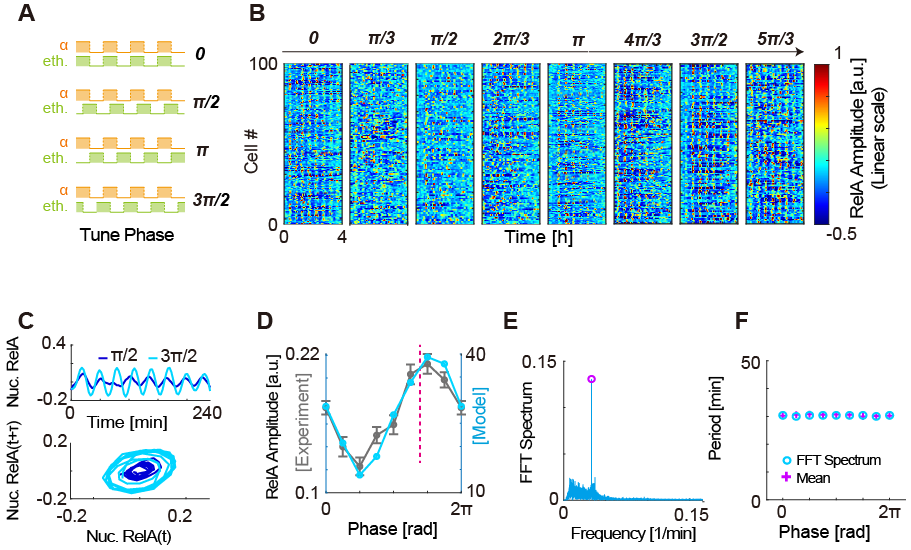
圖5 調控外界周期信號相位實現調幅不調頻
最后,通過引入下游熒光報告基因,作者在實驗和模型中確認了這種相位調整帶來的振幅變化的確能造成基因表達水平的差異。這種差異與振蕩的基線水平、振蕩周期均無關。
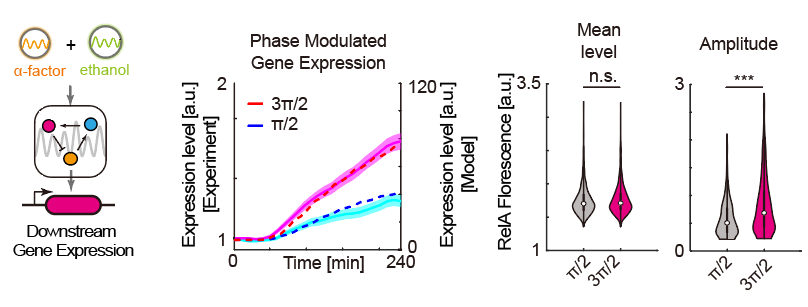
圖6 通過改變外界周期信號間相位差,調控基因表達
本項研究首次同時在實驗和理論水平揭示了多耦合振蕩系統中的協同性現象,發現了這類系統中獨特的相位調控原理,拓寬了學界對于生物耦合振蕩系統的認識,以及對生物學中時間調控的理解。本研究中構建的雙輸入人工合成振蕩系統,可為后續進一步探索多耦合振蕩中的基本問題提供穩健、可靠的實驗平臺。這種從根本上理解生命系統設計原理的工作,為人工設計合成生命、理解復雜疾病的發生機理提供了重要的理論基礎。
哥本哈根波爾研究所Mathias S. Helberg博士(中科院深圳先進院訪問學者)、北京大學定量生物學中心博士研究生姜源旭(中科院深圳先進院客座學生)、中科院深圳先進院博士后范盈盈(原北京大學定量生物學中心博士)為本文的共同第一作者。中科院深圳先進院魏平研究員與哥本哈根大學玻爾研究所Mogens H. Jensen教授為本文的共同通訊作者。北京大學定量生物學中心歐陽頎院士、錢瓏研究員對本項研究提供了寶貴的指導和意見。北京大學定量生物學中心博士研究生林維、原北京大學定量生物學中心博士張志博對本研究的前期結果提供了重要貢獻。本項研究獲得了國家科技部重點研發計劃項目、國家自然科學基金項目、中國科學院戰略重點研究項目及深圳合成生物學創新研究院等項目的支持。
參考文獻
1. Yoshioka-Kobayashi, K., Matsumiya, M., Niino, Y., Isomura, A., Kori, H., Miyawaki, A., & Kageyama, R. (2020). Coupling delay controls synchronized oscillation in the segmentation clock. Nature, 580, 119-123.
2. Mondragón-Palomino, O., Danino, T., Selimkhanov, J., Tsimring, L.S., & Hasty, J. (2011). Entrainment of a Population of Synthetic Genetic Oscillators. Science, 333, 1315 - 1319.
3. Zhang, Z., Wang, Q., Ke, Y., Liu, S., Ju, J., Lim, W.A., Tang, C., & Wei, P. (2017). Design of Tunable Oscillatory Dynamics in a Synthetic NF-κB Signaling Circuit. Cell systems, 5 5, 460-470.e5 .
附件下載:


