很多疾病的發生發展呈現性別偏好性(Sex bias),但機制尚不清楚,前期研究表明干細胞的性別維持和紊亂可能是疾病性別偏好的新機制。干細胞如何協調胞內外信號以維持性別特征從而保持組織穩態是關鍵問題。盡管目前對性別決定機制以及胚胎發育期間體細胞的性別對生殖細胞的影響已有廣泛報道,但成年期干細胞性別身份維持的分子機制以及體細胞與生殖細胞之間的相關信號在很大程度上仍未被探索。
2024年6月22日,中國科學院深圳先進技術研究院合成生物學研究所、深圳合成生物學創新研究院馬晴課題組和中山大學生命科學院徐錦課題組在National Science Review雜志在線發表了題為Soma-Germline Communication Drives Sex Maintenance in the Drosophila?Testis的最新研究成果。
?

文章上線截圖,鏈接:https://doi.org/10.1093/nsr/nwae215
?
該研究利用果蠅精巢干細胞性別轉變導致的雄性特異的生殖系統腫瘤模型,聯合應用scRNA-Seq和CUT&Tag技術表明了成年果蠅體干細胞(Somatic cyst stem cells,CySCs)的性別維持(Sex maintenance)通過Chinmo蛋白的非編碼突變介導的保守性別決定信號通路(Sex determination pathway)和胰島素信號通路(Insulin signaling pathway)調控。該研究在單細胞水平解析了“性別開關”Chinmo的非編碼突變導致的果蠅精巢體干細胞雌性化的分子特征,揭示了體細胞-生殖細胞間通訊異常導致生殖細胞性別紊亂和腫瘤化的信號傳導機制。該研究強調了干細胞性別不穩定性作為導致生殖系統腫瘤發生的新機制的潛在重要性,并為理解腫瘤發生和不孕癥背后的復雜機制提供了新見解。
?
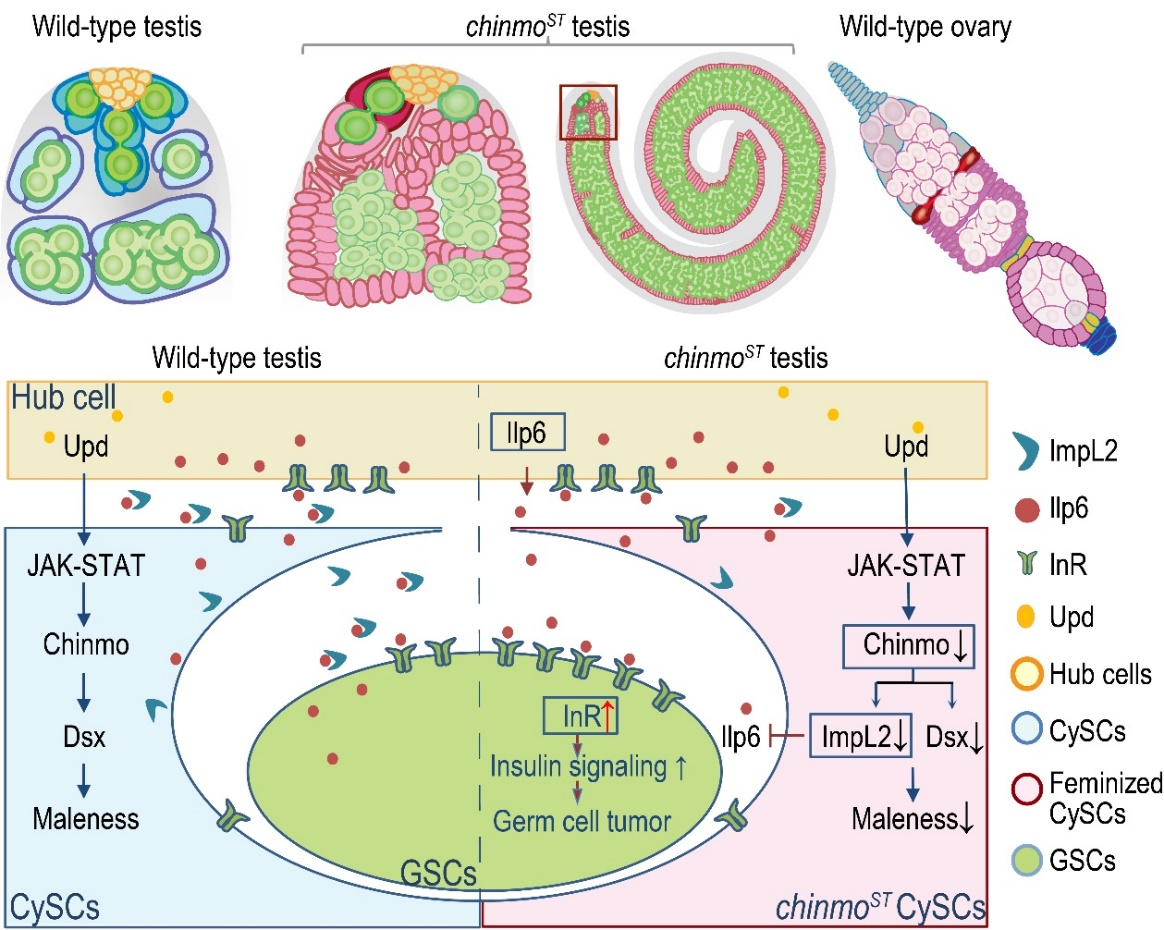
圖1:"性別開關"Chinmo受JAK-STAT信號通路的調控,直接作用于雄性性別決定因子DsxM(果蠅中與哺乳動物性別決定因子DMRT1同源的基因)和胰島素信號通路因子,以維持CySC譜系的雄性身份并促進正常的精子發生。
在許多生物中,細胞性別身份在胚胎發育期間就已建立且在過去認為其性別是不可改變的,但最近的研究發現成年性腺中體干細胞的性別也可以發生轉變,這表明體細胞的性別身份在成年期或出生后是需要維持的。那么成年期的(干)細胞是如何維持其性別身份,以及體細胞與生殖細胞之間是如何相互作用以維持正常的配子發生呢? 作者前期報道了一種果蠅精巢突變表型,其體干細胞在成年期發生性別轉變,為研究體細胞的性別維持以及體細胞-生殖細胞間通訊提供了一個合適的模型。作者前期發現JAK-STAT信號通路的關鍵效應因子和“性別開關”Chronologically inappropriate morphogenesis (Chinmo)的非編碼突變(chinmoSex Transformation,chinmoST)誘導了CySCs的性別逆轉進而導致雄性偏好的腫瘤發生。由于只有少量性別特異性體細胞標記物,無法全面解析隨時序發生轉分化的體干細胞的譜系軌跡以及不同體細胞和生殖細胞的分子特征。此外,Chinmo誘導的“性別轉變”體干細胞與本應“雄性”的生殖細胞之間的信號通訊又是否發生了變化呢?
?
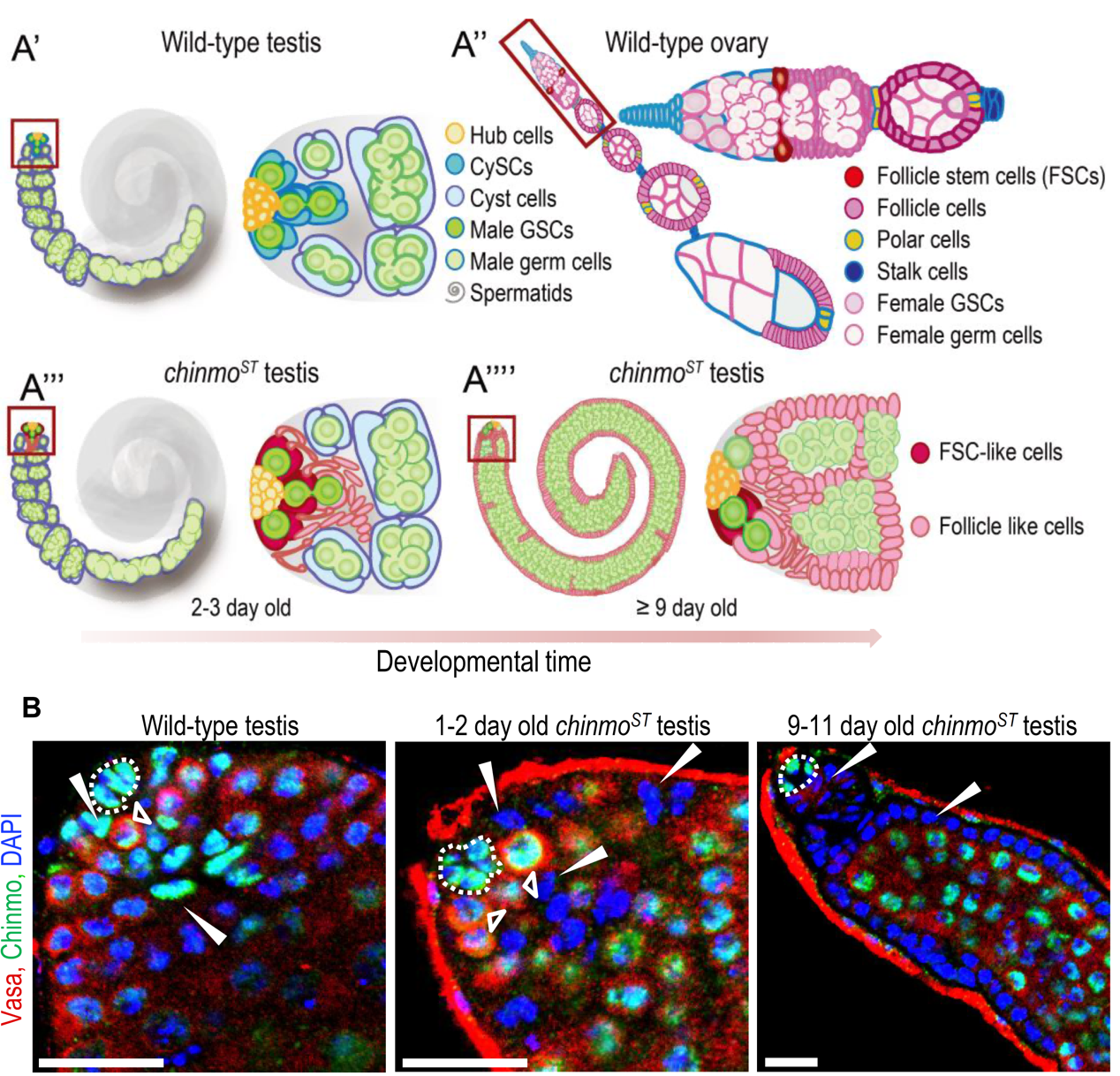
圖2:野生型精巢、chinmoST突變型精巢和野生型卵巢示意圖,以及野生型和chinmoST突變型精巢染色圖
圍繞上述問題,作者對成年果蠅的多個發育時段的精巢進行了單細胞RNA測序(scRNA-seq)來表征野生型和chinmoST突變精巢的轉錄組圖譜。作者鑒定了chinmoST特有的細胞群體,并檢測到了與表型相對應的轉錄組變化。通過比較分析野生型和chinmoST突變精巢之間的細胞間通訊網絡(Cell-cell communication network),發現包括胰島素信號通路在內的幾個體細胞-生殖細胞間信號通路在chinmoST突變精巢中發生了紊亂,其中胰島素信號通路從雌性化的CySCs到生殖細胞干細胞(GSCs)之間的信號傳導顯著增強。Chinmo CUT&Tag(Cleavage Under Targets and Tagmentation)檢測分析揭示了Chinmo直接調控兩個雄性性別決定因子,doublesex(dsx)和fruitless(fru),以及胰島素信號通路的調控因子。進一步的果蠅遺傳實驗確認了在chinmoST突變精巢中觀察到的配子發生障礙的部分原因是由于胰島素通路信號的失調。總之,研究表明體細胞維持性別是通過Chinmo介導的保守性別決定通路和胰島素信號通路共同促進了正常的配子發生。
?
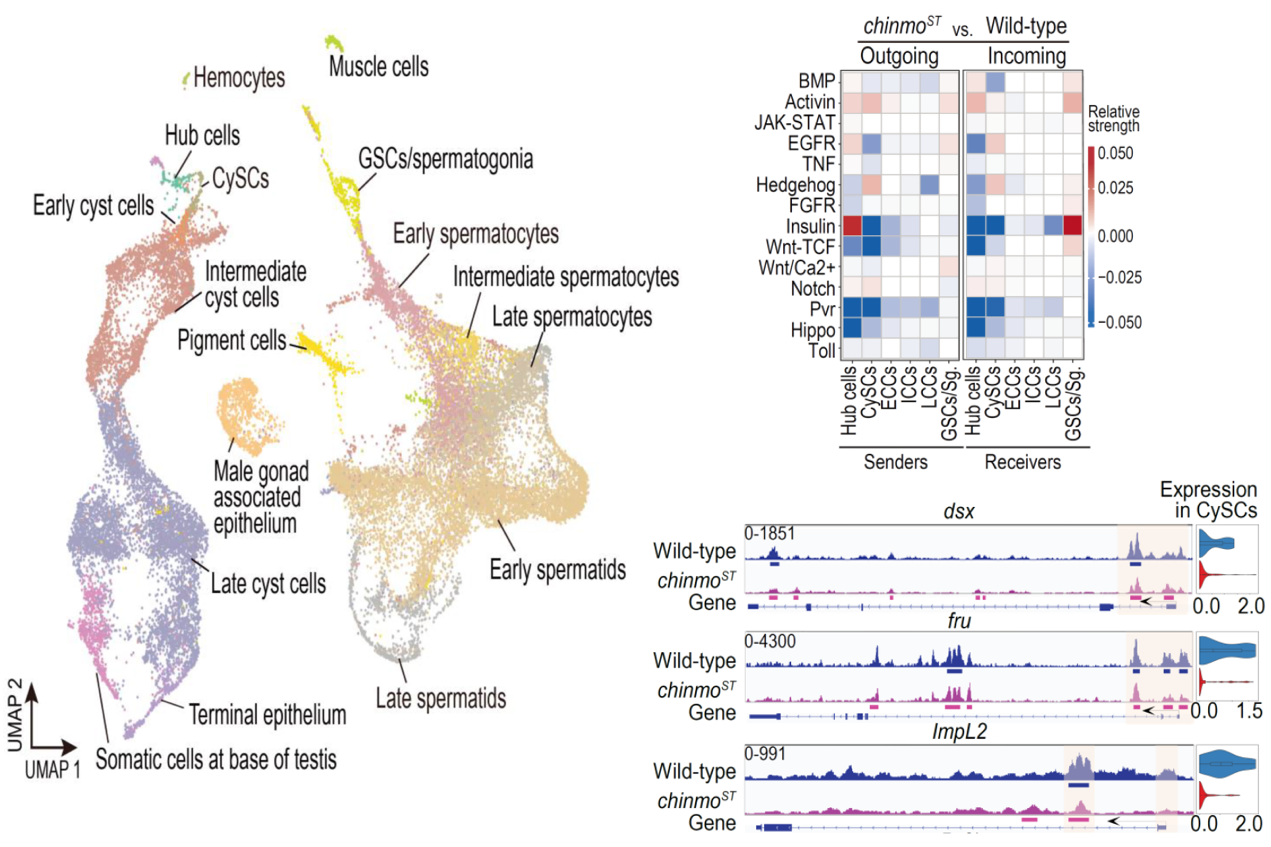
圖3:成年果蠅精巢單細胞數據圖,精巢細胞間的信號傳導,以及Chinmo靶基因示例
?
這一發現為體干細胞性別維持和單細胞水平上的體細胞-生殖細胞通訊的復雜機制提供了新的見解,為理解不孕癥背后的復雜機制提供了新的視角,強調了干細胞性別維持的不穩定性與睪丸腫瘤發生、生育能力受損之間的直接聯系。另外,作者前期還發現“性別開關”Chinmo能被一些非編碼元件調節,在果蠅生殖干細胞中心行使調控干細胞性別和生殖系統腫瘤發生的功能,這也暗示著非編碼調控在干細胞性別維持和性別偏好疾病發生過程中的重要作用。更為重要的是,許多疾病的發生發展具有明顯的性別偏向性,如自身免疫疾病、神經系統疾病、心血管疾病、感染類疾病(包括新冠肺炎COVID-19),甚至多種癌癥。傳統的疾病治療手段往往忽略了性別因素,有時會導致疾病治療效果表現出性別差異性響應。全面解析干細胞性別維持的分子機制及其介導的細胞間相互作用有望為性別偏好的疾病防治提供新的靶點。
?
中國科學院深圳先進技術研究院合成生物學研究所研究員馬晴和中山大學生命科學院教授徐錦為本文的共同通訊作者。中國科學院深圳先進技術研究院助理研究員張睿,研究助理施佩瑜(原中山大學碩士研究生)為共同第一作者。本工作獲得了科技部重點研發計劃、國家自然科學基金、廣東省基礎與應用基礎研究基金、廣東省合成基因組學重點實驗室、深圳市合成基因組學重點實驗室等多個項目的經費支持。
附件下載:


