微納生物機器人具有行為精準可控、功能多樣性及優(yōu)異的生物相容性等特點,是實現(xiàn)精準醫(yī)療和復雜生物任務(wù)的理想工具。然而,如何有效地控制其運動和功能成為研究的關(guān)鍵。超聲在深層生物組織中具有良好的穿透性,能夠?qū)崿F(xiàn)非侵入式、遠程的精確操控,對生物體安全性高。因此,超聲驅(qū)動在微納生物機器人領(lǐng)域具有重要的應(yīng)用潛力。
北京時間12月21日,中國科學院深圳先進技術(shù)研究院醫(yī)藥所蔡林濤團隊和醫(yī)工所馬騰團隊聯(lián)合在國際學術(shù)期刊《Trends in Biotechnology》上發(fā)表了題為“Programmable Ultrasound-Mediated Swarms Manipulation of Bacteria-Red Blood Cell Microrobots for Tumor-Specific Thrombosis and Robust Photothermal Therapy”的文章。該工作成功開發(fā)了一種具有自主缺氧感知和超聲響應(yīng)功能的細菌-細胞生物機器人,通過缺氧靶向聯(lián)合超聲操控,實現(xiàn)腫瘤深層滲透和生成腫瘤特異性血栓,最終實現(xiàn)高效精準治療。

https://authors.elsevier.com/c/1kIeKc9XEnKgD
該研究利用光合細菌獨特的缺氧感知能力和自身分泌細菌葉綠素的特性,結(jié)合紅細胞雙凹圓盤結(jié)構(gòu)的特點,構(gòu)建了一種光合細菌-紅細胞偶聯(lián)的生物微型機器人(PR-robot)。該生物機器人具有較長的體內(nèi)循環(huán)時間,并自主靶向腫瘤區(qū)域,提高了腫瘤特異性富集效率。同時,紅細胞的特殊結(jié)構(gòu)增強了PR-robot的聲阻抗,使PR-robot能夠以生物集群方式被超聲鑷精確控制和驅(qū)動,甚至穿越生物屏障、深度滲透到腫瘤組織內(nèi)部。生物群的涌入誘導腫瘤特異性血栓的形成,協(xié)同光合細菌增強光熱抗腫瘤效果。
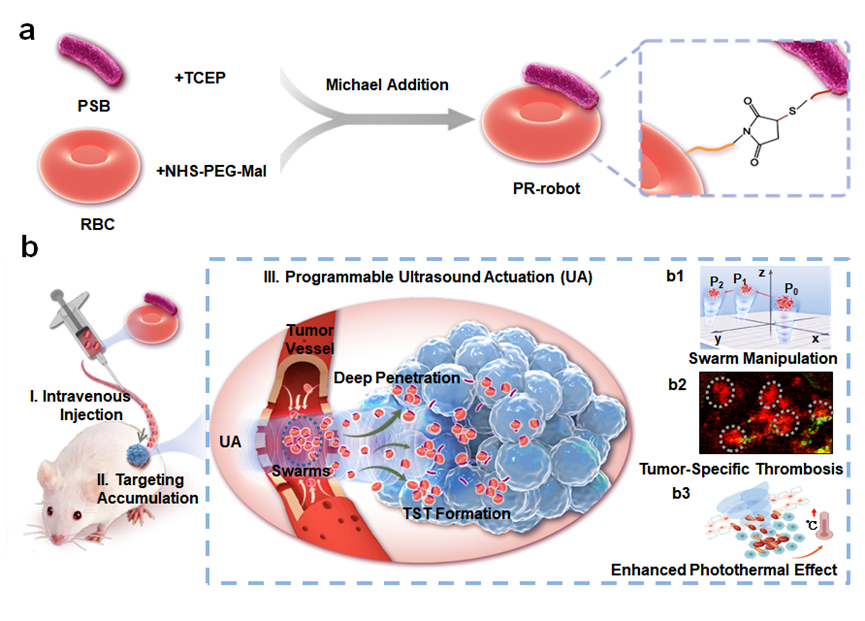
超聲驅(qū)動細菌-紅細胞微型生物機器人實現(xiàn)深度滲透用于癌癥治療
研究團隊進行了一系列體外和體內(nèi)實驗,以驗證生物群的超聲可控性和深度滲透的有效性以及生物安全性。首先通過NHS-PEG2000-Mal和- SH的邁克爾加成偶聯(lián)制備了PR-robots。隨后在體外利用程序化超聲驗證了對這些生物機器人的捕獲和驅(qū)動能力。研究顯示,超聲鑷能夠抓取PR-robots形成生物群集,同時還能精準操控生物群沿著既定路線自主運動,甚至在逆流中前進。進一步研究顯示,生物群在超聲操控下,能夠有序穿越屏障,實現(xiàn)深度滲透。在體內(nèi)研究中,PR-robots被尾靜脈注射后,能夠利用細菌的缺氧感知能力和紅細胞的保護作用,高效靶向到腫瘤區(qū)域。超聲鎳捕獲這些PR-robots,并驅(qū)動生物群向腫瘤組織內(nèi)部滲透。隨著PR-robots的涌入,腫瘤組織內(nèi)部形成大量腫瘤特異性血栓,協(xié)同增強光熱治療效果。該微型生物機器人的開發(fā)為基于超聲驅(qū)動控制的藥物深層遞送和相關(guān)疾病的治療提供了全新的技術(shù)手段和設(shè)計理念。
中國科學院深圳先進技術(shù)研究院蔡林濤研究員、馬愛青副教授、馬騰研究員、劉蘭蘭副研究員為通訊作者,碩士研究生冉慧、博士后楊曄、韓偉靜副研究員和梁銳晶副研究員為共同第一作者。該研究工作得到了國家自然科學基金委、科技部、廣東省科技廳、深圳市科創(chuàng)委等科技項目的資助。
附件下載:


