近日,中國科學院廣州生物醫藥與健康研究院等機構在Cell Reports Medicine發表題為“CD4+?anti-TGFβ CAR T cells and CD8+?conventional CAR T cells exhibit synergistic antitumor effects”的研究論文。該研究首次證實CD4+靶向TGFβ的CAR-T細胞(T28zT2 T細胞)與CD8+靶向GPC3或MSLN的CAR-T細胞聯合應用具有協同抗腫瘤效應,為實體瘤免疫治療提供了全新策略,并同步啟動針對肝癌和胰腺癌等實體瘤的相關臨床研究(NCT03198052)。
TGFβ1是腫瘤微環境中的關鍵抑制性因子,可抑制CD4+?T細胞、CD8+?T細胞及NK細胞的效應功能。然而,TGFβ1也能夠通過促進CD8+?T細胞重編程為組織駐留記憶T細胞(Trm細胞),增強其續存和定植能力。這表明TGFβ信號具備高度的亞群依賴性,即可作為抑制性因子,也能通過特定途徑重塑T細胞功能。
研究團隊研發了一款新型靶向TGFβ的CAR-T細胞(T28zT2 T細胞),通過中和TGFβ信號逆轉腫瘤微環境中的免疫抑制,并展現出顯著的抗腫瘤潛力。研究發現,CD4+?T28zT2細胞在TGFβ1刺激下可在血液和腫瘤中長期存活,并分泌Granzyme B和IFN-γ直接殺傷腫瘤;而CD8+?T28zT2 T細胞則未顯示同等抗腫瘤效應。進一步分析表明,腫瘤浸潤的CD4+?T28zT2細胞高表達TCF-1、IL7R和CXCR3,呈現記憶樣T細胞特征,同時上調NKG2D并降低PD-1/LAG3等耗竭標志物,顯著增強其抗腫瘤活性。此外,CD4+?T28zT2細胞能夠重塑腫瘤微環境,協同增強靶向GPC3或MSLN的CD8+?CAR-T細胞的抗腫瘤能力,呈現倍增效應。
機制研究揭示,CD4+?T28zT2細胞通過阻斷TGFβ1誘導的線粒體分裂和膜電位抑制維持效應功能,同時通過CXCR3高表達促進腫瘤浸潤,NKG2D的上調則精準遞送殺傷因子以避免全身毒性。基于這一突破,團隊已啟動相關臨床研究(NCT03198052),旨在評估“CD4+靶向TGFβ CAR-T聯合CD8+靶向MLSN或GPC3 CAR-T”治療惡性實體腫瘤的安全性和有效性。該療法有望突破目前實體瘤CAR-T細胞療法響應率低、復發率高的瓶頸,推動CAR-T細胞療法在實體瘤領域的臨床轉化。
廣州健康院李鵬研究員為論文的唯一通訊作者。中國科學院香港創新研究院再生醫學與健康創新中心鄭迪威博士、廣州健康院秦樂副研究員為共同第一作者。研究項目得到了國家重點研發計劃、國自然以及GIBH自主部署項目等經費的支持。
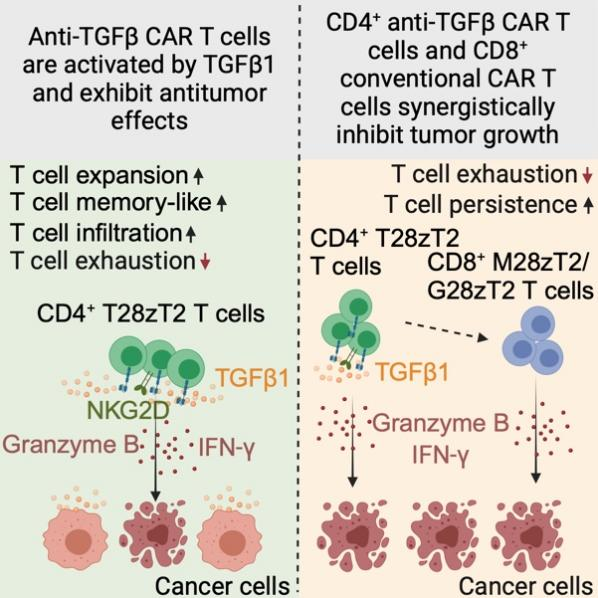
圖1?CD4+靶向TGFβ CAR-T細胞具備殺傷癌細胞和協同抗癌雙重作用
附件下載:


