近日,中國科學(xué)院廣州生物醫(yī)藥與健康研究院李鵬研究員和孔祥謙研究員團(tuán)隊在Science Immunology發(fā)表題為"DNMT1 inhibition reprograms T cells to NK-like cells with potent antitumor activity"的研究論文。該研究揭示了DNA甲基轉(zhuǎn)移酶DNMT1通過表觀遺傳與蛋白質(zhì)互作雙重機(jī)制維持T細(xì)胞身份的關(guān)鍵作用,研發(fā)了通過表觀遺傳小分子抑制劑將T細(xì)胞誘導(dǎo)重編程為同時具有T細(xì)胞和NK細(xì)胞功能的NK樣細(xì)胞,有望為癌癥免疫細(xì)胞治療提供一種新細(xì)胞源。
T細(xì)胞和NK細(xì)胞都是重要的免疫細(xì)胞。T細(xì)胞主要參與適應(yīng)性免疫應(yīng)答,而NK細(xì)胞是天然免疫系統(tǒng)的一部分,具有直接殺傷腫瘤細(xì)胞和病毒感染細(xì)胞的能力。它們在腫瘤免疫中體現(xiàn)出高度的互補性:T細(xì)胞可識別表達(dá)MHC-I的癌細(xì)胞,NK細(xì)胞則通過NK細(xì)胞受體(NCR)來識別MHC-I缺失的癌細(xì)胞。
BCL11B是T細(xì)胞譜系發(fā)育和T細(xì)胞身份維持的關(guān)鍵轉(zhuǎn)錄因子。研究團(tuán)隊首先發(fā)現(xiàn)DNMT1/UHRF1復(fù)合物與BCL11B存在相互作用,且DNMT1通過N端結(jié)構(gòu)域直接結(jié)合BCL11B的鋅指結(jié)構(gòu)域,阻止其被泛素化降解。進(jìn)一步發(fā)現(xiàn),BCL11B通過招募DNMT1/UHRF1復(fù)合物到NK細(xì)胞相關(guān)基因的啟動子區(qū)域,導(dǎo)致該區(qū)域的DNA甲基化修飾,從而抑制相關(guān)基因的轉(zhuǎn)錄。
闡明BCL11B與DNMT1協(xié)同維持T細(xì)胞身份分子機(jī)理后,研究團(tuán)隊對人外周血來源的T細(xì)胞用DNMT1的選擇性抑制劑GSK862進(jìn)行處理,導(dǎo)致BCL11B和DNMT1的蛋白降解,從而導(dǎo)致NKp30和NKp46等多種NK細(xì)胞特征性基因的轉(zhuǎn)錄上調(diào),使得T細(xì)胞表現(xiàn)出NK細(xì)胞的功能,能夠通過分泌穿孔素、顆粒酶B等效應(yīng)分子來殺傷腫瘤細(xì)胞。
聯(lián)合使用DNMT1的選擇性抑制劑和組蛋白修飾酶EZH2的抑制劑可以進(jìn)一步提升NK樣細(xì)胞重編程效率和抗腫瘤活性。這種由表觀遺傳小分子抑制劑組合誘導(dǎo)獲得的NK樣細(xì)胞在人源化小鼠模型中展現(xiàn)出優(yōu)異的抗腫瘤活性。CAR-T細(xì)胞也可通過同樣的方法被誘導(dǎo)重編程為識別癌抗原更廣泛,抗腫瘤活性更強的CAR-NK樣細(xì)胞。
綜上所述,本項研究首次揭示了轉(zhuǎn)錄因子BCL11B與表觀調(diào)控復(fù)合體DNMT1/UHRF1協(xié)同維持T細(xì)胞身份的核心機(jī)制,并基于此開發(fā)了一種新型T細(xì)胞重編程技術(shù),成功將其轉(zhuǎn)化為具有腫瘤殺傷功能的NK樣細(xì)胞。該研究為腫瘤的臨床免疫細(xì)胞治療提供了潛在來源,同時也為解析T細(xì)胞發(fā)育過程中的表觀遺傳調(diào)控提供了新的視角。
廣州健康院李鵬研究員和孔祥謙研究員為該論文的共同通訊作者,博士后李搖、博士生王炯亮、博士后周林付和助理研究員顧文彬博士為共同第一作者。該研究得到了香港大學(xué)劉澎濤教授、廣州健康院王杰研究員的大力幫助。研究項目得到了國家重點研發(fā)計劃、國自然以及GIBH自主部署項目等經(jīng)費的支持。
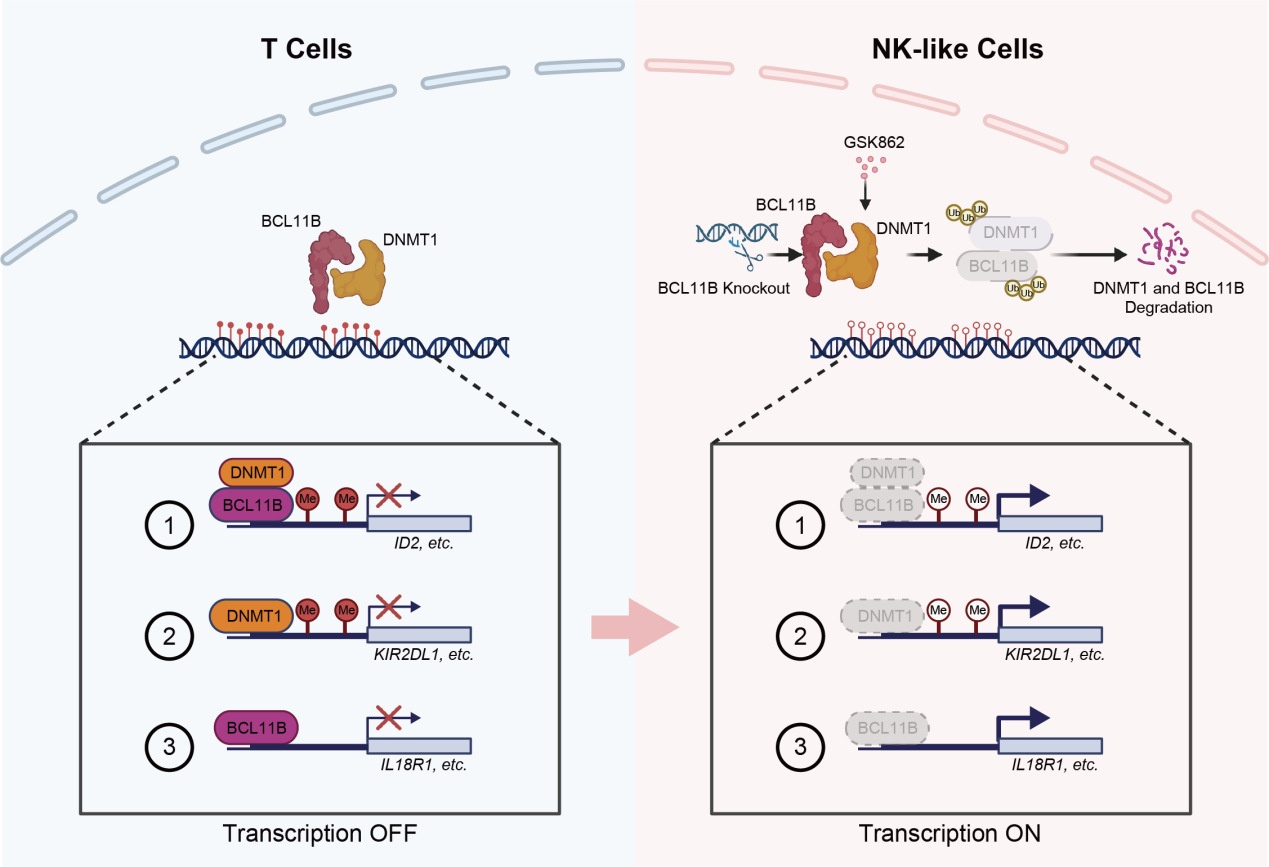
圖1?BCL11B與DNMT1協(xié)同抑制NK細(xì)胞相關(guān)基因表達(dá),維持T細(xì)胞身份
附件下載:


