2025年7月15日,中國科學院廣州生物醫(yī)藥與健康研究院彭廣敦課題組和廣州國家實驗室索生寶課題組合作,在Nature Communications上發(fā)表了題為High-resolution mapping of single cells in spatial context的研究論文。
細胞是生命的基本結(jié)構(gòu)和功能單元,其活動不僅受胞內(nèi)基因網(wǎng)絡調(diào)控,還受到胞外微環(huán)境和細胞間通訊的影響。單細胞轉(zhuǎn)錄組測序技術(shù)為解析細胞異質(zhì)性帶來了革命性突破,但這一技術(shù)在細胞捕獲過程中丟失了空間位置信息,嚴重限制了我們對細胞命運決定和調(diào)控機制的深入理解。
近年來,空間轉(zhuǎn)錄組技術(shù)迅速發(fā)展,成為揭示組織微環(huán)境中細胞狀態(tài)與相互作用的重要工具。然而,現(xiàn)有技術(shù)在細胞尺度的分辨率和全轉(zhuǎn)錄本覆蓋度方面仍面臨挑戰(zhàn),亟需計算方法對單細胞數(shù)據(jù)進行精準的空間重建。
針對這一問題,研究團隊提出了CMAP(Cellular Mapping of Attributes with Position)計算模型,通過整合單細胞和空間轉(zhuǎn)錄組數(shù)據(jù),采用“分治”策略,實現(xiàn)大規(guī)模單細胞向空間位置的高精度映射。

CMAP借鑒“地圖導航”式的搜索策略,逐步將細胞精準定位于組織空間中(圖1):
1.?DomainDivision:通過提取空間數(shù)據(jù)的粗粒度特征,將細胞初步分配至大的空間區(qū)域;
2.?OptimalSpot:在區(qū)域內(nèi)搜索與該細胞表達特征最匹配的空間樣本點;
3.?PreciseLocation:進一步結(jié)合該樣本點及其鄰域的空間組織特征,利用彈簧平衡態(tài)模型,推斷細胞的精確坐標。
這一分層映射策略使得CMAP能夠在保證計算效率的同時,實現(xiàn)單細胞分辨率的空間表達圖譜重構(gòu)。
為系統(tǒng)評估CMAP的預測性能,CMAP在多組模擬數(shù)據(jù)和高分辨率Xenium空間數(shù)據(jù)上進行測試。通過比較不同方法的預測精度、細胞類型占比及重構(gòu)的空間基因表達模式,結(jié)果表明CMAP在預測準確性和重構(gòu)效果方面均優(yōu)于現(xiàn)有方法CellTrek和CytoSPACE。特別是通過彈簧平衡態(tài)模型優(yōu)化,CMAP能夠提供單細胞級空間坐標,突破了大多數(shù)方法仍停留在spot水平上的局限,實現(xiàn)真正的單細胞空間重構(gòu)。此外,CMAP在不同數(shù)據(jù)質(zhì)量和不同技術(shù)來源的多種應用場景中表現(xiàn)出兼容性與魯棒性,能夠有效解決特定細胞的空間定位和非匹配細胞的過濾問題,而CellTrek和CytoSPACE則在此類場景中存在明顯不足。在真實生物學問題中,CMAP在彭廣敦課題組發(fā)表的Geo-seq數(shù)據(jù)以及小鼠13.5天胚胎空間轉(zhuǎn)錄組數(shù)據(jù)中均展示了優(yōu)異的空間位置特異定位能力,也揭示了胚胎內(nèi)皮細胞的組織異質(zhì)性。此外,CMAP還成功重構(gòu)了腫瘤免疫微環(huán)境中的三級淋巴結(jié)構(gòu)(Tertiary lymphoid structures,TLS),揭示了T/B細胞在空間上共定位和相互作用,并基于空間坐標實現(xiàn)了高分辨率的細胞互作分析。
綜上所述,本研究構(gòu)建了單細胞空間位置推斷模型CMAP,建立了“單細胞-空間-功能”的多維解析框架,推動了單細胞轉(zhuǎn)錄組與空間組學的深度融合,為疾病機制解析和精準醫(yī)學發(fā)展提供了新的研究思路。
中國科學院廣州生物醫(yī)藥與健康研究院彭廣敦研究員和廣州國家實驗室索生寶研究員為該論文共同通訊作者,廣州健康院博士研究生柯今燦為論文第一作者。
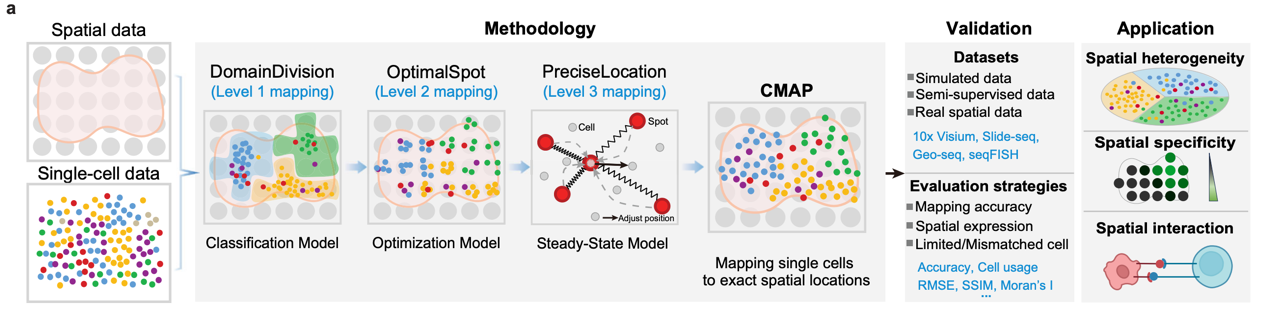
圖1. CMAP方法的框架設計
附件下載:


