近日,中科院深圳先進院集成技術研究所神經工程中心李光林研究員團隊的唐為副研究員課題組聯合上海交通大學氫科學中心何前軍教授合作在Science Advances發表題為“NIR-photocatalytic regulation of arthritic synovial microenvironment”的文章。文章上線后就立即收到了Nature Reviews Rheumatology雜志副主編Dr Robert Philips的采訪,并為該工作撰寫Research highlights,認為催化調控微環境“使風濕性關節炎的無藥治療成為可能”。深圳先進院唐為副研究員與上海交通大學何前軍教授為共同通訊作者。中國科學院深圳先進技術研究院、上海交通大學與深圳大學為該論文共同通訊單位。
類風濕性關節炎(RA)是一種自身免疫性疾病,伴隨慢性炎癥,常導致手足關節畸形及功能喪失,被稱為“不死的癌癥”。其中關節炎滑膜微環境誘導的滑膜增生、血管翳形成及軟骨侵蝕,在RA的病理發展進程中發揮著至關重要的作用。非甾體抗炎藥、抗風濕藥、糖皮質激素是目前RA治療的常用藥物,但都存在毒副作用大、無法調控骨免疫失衡、難以阻止RA進程等系列問題,使得RA治療亟需新的有效干預手段。
該工作提出了光催化調控關節炎滑膜微環境的新概念,并通過全溶液法開發了一種具有金紅石單晶結構的單分散氫摻雜二氧化鈦納米催化劑,有效實現了近紅外光催化產氫和乳酸剝奪,從而聯合校正了滑膜微環境(如下圖所示),達到了高效的RA治療效果。一方面,原位產生的氫分子通過清除過表達ROS,介導巨噬細胞抑炎極化;另一方面,將RA微環境中過表達的代謝中間產物乳酸轉化為丙酮酸,進一步抑制了滑膜細胞和巨噬細胞的炎癥/侵襲型轉變,降低滑膜細胞異常增殖,防止滑膜血管翳的形成。小鼠膠原誘導關節炎模型實驗結果證實該策略可有效阻止RA病程的加劇,顯著減少軟骨破壞及骨侵蝕。該研究工作通過可控、按需釋氫,同時原位消耗過表達乳酸的新方法,有望為RA臨床治療提供重要的技術支撐和科學價值。
該工作得到了中國科學院人機智能協同系統重點實驗室、國家自然科學基金、深圳市科創委、中國科學院青年創新促進會以及上海交通大學氫科學中心等基金項目的支持。

圖1 文章線上截圖
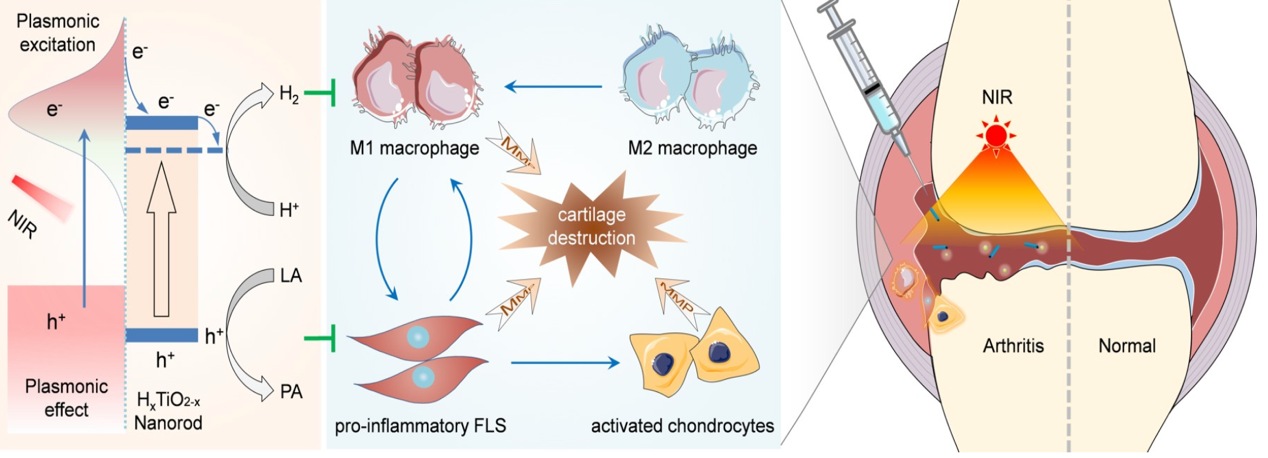
圖2 光催化調控關節炎滑膜微環境策略,原位催化產氫和乳酸剝奪,介導過表達病理產物清除,實現可控、按需、高效RA治療。
全文鏈接
https://www.science.org/doi/10.1126/sciadv.abq0959
附件下載:


